马飞教授:新型抗 HER2 ADC 为 HER2 低表达乳腺癌带来新希望|SABCS 2023
第 46 届圣安东尼奥乳腺癌研讨会(SABCS)于 12 月 5-9 日在美国圣安东尼奥召开,作为全球乳腺癌领域最为重要的国际学术会议之一,本届 SABCS 大会将继续聚焦乳腺癌和癌前乳腺疾病的实验生物学,病因学,预防,诊断和治疗最新进展,提供学术交流互动和继续教育平台。
在本届 SABCS 大会上,加州大学旧金山分校 Pamela Munster 教授分享了题为 「Report on Cohort Expansion of Phase I Study to Investigate the Safety, Tolerability, Pharmacokinetics and Antitumor Activity of BB-1701 in Patients with Locally Advanced/Metastatic HER2 Low Breast Cancer」 的报告,介绍了正在进行的 BB-1701 治疗 HER2 低表达乳腺癌患者的 I 期研究的初步结果。该研究为中国医学科学院肿瘤医院马飞教授牵头的一项国际多中心研究。

图 1:汇报课题
研究背景
BB-1701 是一种抗体药物偶联物 (ADC),由与曲妥珠单抗序列相同的人源化 IgG1κ 单克隆抗 HER2 抗体和艾立布林组成,通过组织蛋白酶可裂解的缬氨酸-瓜氨酸连接子连接在一起。艾立布林是一种微管抑制剂,已被批准用于治疗转移性乳腺癌和晚期脂肪肉瘤。当 BB-1701 作用到靶向表达 HER2 的癌细胞并被内吞时,游离的艾立布林会被组织蛋白酶 b 从 ADC 中裂解出来,从而对癌细胞产生细胞毒性。临近细胞会受到旁观者效应的影响,例如垂死癌细胞释放的游离艾立布林对肿瘤细胞的细胞毒性和对微环境的非细胞毒性作用。
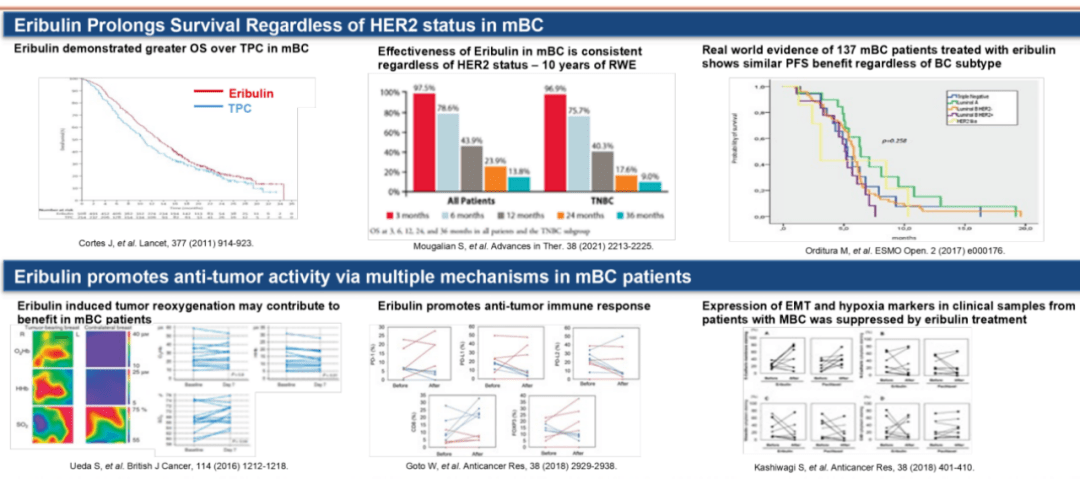
图 2:研究背景
研究设计及方法
该研究纳入了年龄 ≥18 岁、确诊为局部晚期/转移性 HER2 低表达乳腺癌(IHC 2+且 FISH 阴性或 IHC 1+)的患者,这些患者既往至少接受过两线标准疗法且病情进展、ECOG PS≤2 且存在可测量病灶(RECIST 1.1)。入组前研究人员通过 IHC 和 FISH 检测来确认患者 HER2 表达情况。在队列扩展期间,共使用了四种剂量水平的 BB-1701,分别为 1.0 mg/kg Q3W、1.2 mg/kg Q3W、1.4 mg/kg Q3W 和 1.6 mg/kg Q3W。该研究主要评估了不同剂量 BB-1701 的安全性、耐受性和初步抗肿瘤活性,每 6 周进行一次放射学评估。此前,马飞教授团队在今年 ASCO 会议上已报告 BB-1701 治疗 HER2 过表达实体瘤患者的Ⅰ期研究的初步结果。
研究结果
截至 2023 年 11 月 8 日,共有 40 例 HER2 低表达乳腺癌患者入组并接受四种不同剂量的 BB-1701 治疗,其中 5 例患者接受 1.0 mg/kg Q3W,20 例患者接受 1.2 mg/kg Q3W,5 例患者接受 1.4 mg/kg Q3W,10 例患者接受 1.6 mg/kg Q3W。入组患者中位年龄为 55 岁(范围 30-74),97.5% 为女性,ECOG PS 为 0(30%)或 1 分(70.0%),既往接受过系统治疗的中位线数为 3 次(范围 2-9)。
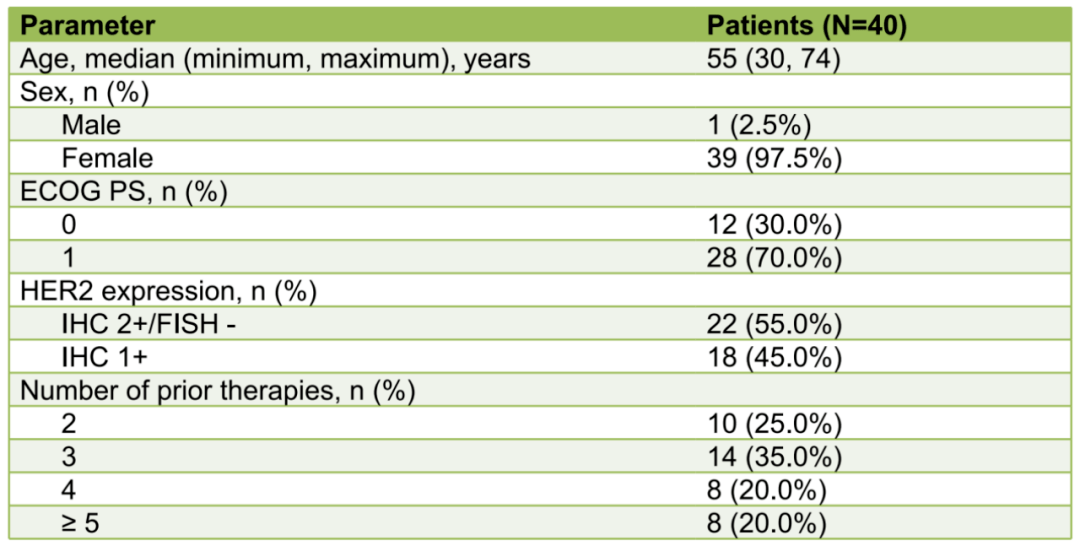
图 3:研究纳入人群基本临床特征
疗效方面
入组的 40 例患者中,38 例患者的抗肿瘤活性可进行评估。
5 例接受 1.0 mg/kg 剂量水平治疗的患者中,4 例为疾病稳定(SD),疾病控制率(DCR)为 80.0%(4/5)。
18 例接受 1.2 mg/kg 剂量水平治疗的患者中,3 例达到 PR,13 例达到 SD,客观缓解率(ORR)为 16.7%(3/18),DCR 为 88.9%(16/18)。
5 例接受 1.4 mg/kg 剂量水平治疗的患者中,1 例达到 PR,3 例达到 SD,ORR 为 20.0%(1/5),DCR 为 80.0%(4/5)。1 例获得 PR 的患者曾在接受戈沙妥珠单抗治疗后出现病情进展。
10 例接受 1.6 mg/kg 剂量水平治疗的患者中,1 例达到完全缓解(CR),2 例达到 PR,3 例达到 SD,ORR 为 30.0%(3/10),DCR 为 60.0%(6/10)。在这些患者中,获得 CR 的患者曾接受过维迪西妥单抗治疗,1 例获得 PR 的患者曾接受过德曲妥珠单抗治疗。
图 4:38 例可评估患者的疗效情况
安全性方面
所有受试者至少出现过一次治疗突发不良事件,其中 30 例受试者出现了治疗相关不良事件(TRAE)。最常见的所有级别 TRAE(≥20%)为周围神经病变、天冬氨酸氨基转移酶升高、丙氨酸氨基转移酶升高、贫血和白细胞计数减少。3 级 TRAE 包括周围神经病变(3 例)、周围感觉神经病变(2 例)、中性粒细胞计数减少(2 例)、血小板计数减少(1 例)和白细胞计数减少(1 例)。此外,还记录了治疗相关的严重不良事件(SAE),分别为周围感觉神经病变、贫血和输液相关反应。在所有受试者中,未观察到 4 级或 5 级事件,也未发生间质性肺病,且没有患者因 AE 停止治疗,安全性良好。
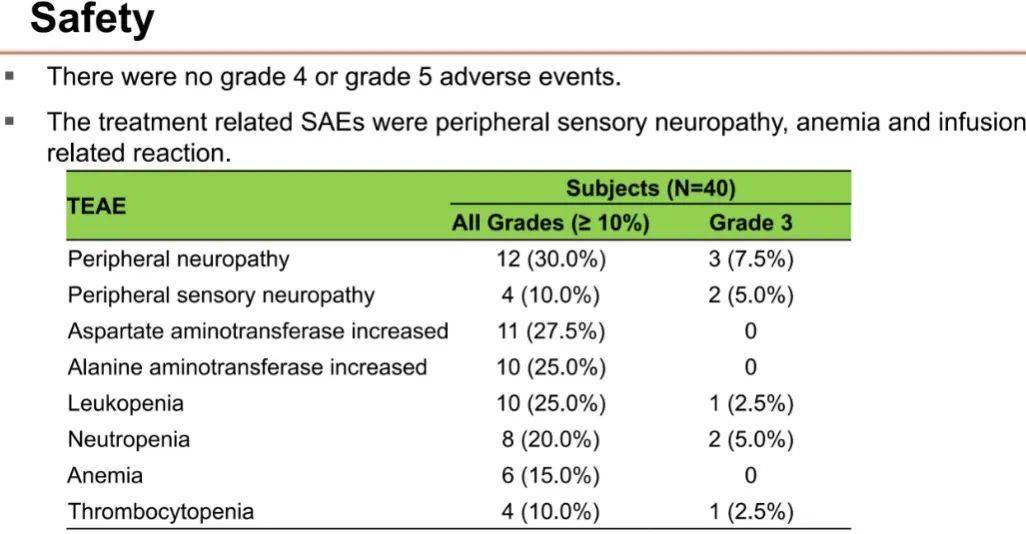
图 5:研究安全性分析
研究结论
总体来说,BB-1701 在 HER2 低表达乳腺癌中表现出良好的初步抗肿瘤活性,并且安全性可控,即使先前接受过抗 HER2 ADC 治疗,BB-1701 仍然能够发挥有效作用。
专家简介

马飞
主任医师 长聘教授 博士生导师
国家癌症中心/中国医学科学院肿瘤医院内科治疗中心主任
教育部长江学者特聘教授
科技部国家重点研发计划首席科学家
国家自然科学基金重点项目负责人
Cancer Innovation 主编
国家肿瘤质控中心乳腺癌专委会副主委
国家癌症中心乳腺癌筛查与早诊早治规范委员会秘书长
国家抗肿瘤药物临床应用监测专委会秘书长
中国药师协会肿瘤专科药师分会副主委
中国抗癌协会整合肿瘤心脏病分会副主委
中国抗癌协会肿瘤药物临床研究专委会秘书长
中国老年学和老年医学学会老年肿瘤分会总干事长
博鳌肿瘤创新研究院理事长
主要研究方向为实体肿瘤内科治疗的临床及转化研究;
在 Lancet oncol、JCO 等知名肿瘤学杂志发表学术论著 100 余篇,编译肿瘤学专著 13 部,主持编写行业指南与规范 12 部;
获得国家科技进步二等奖 1 项,省部级科研奖励 9 项,获得国家专利授权 14 项;
获得 「 首都十大杰出青年医生 」、「 中国肿瘤青年科学家奖 」 等称号。
参考文献:
[1]Pamela Munster,et al. Report on Cohort Expansion of Phase I Study to Investigate the Safety, Tolerability, Pharmacokinetics and Antitumor Activity of BB-1701 in Patients with Locally Advanced/Metastatic HER2 Low Breast Cancer.2023 SABCS, abstract RF02-05.
本文首发于丁香园旗下专业平台:丁香园肿瘤时间
作者:贝塔_内啡肽;审核:马飞教授
编辑:lsh
题图:丁香园创意团队
投稿:luoshuhan@dxy.cn

