标本兼顾,延缓进展:糖肾管理的「破冰」之旅

一项大型横断面调查研究显示,在我国糖尿病患者中 CKD 的总体患病率为 35.5%,患病人群庞大[1]。CKD 的管理强调延缓疾病进展和降低心血管事件风险,改善血糖、血压等危险因素,同时亦需关注 CKD 并发症如肾性贫血等[2]。然而,过去 2 型糖尿病(T2DM)合并 CKD 的治疗手段较少且效果有限。
随着新型药物的不断研发上市,T2DM 合并 CKD 的管理迎来了新突破。2023 年 11 月 24 日,在中华医学会糖尿病学分会(CDS)第二十五次全国学术会议上,北京大学第三医院洪天配教授、华中科技大学同济医学院附属同济医院余学峰教授和南方医科大学南方医院薛耀明教授,带领我们重温了这场「破冰」之旅。
T2DM 合并 CKD 带来双重危害
亟需有效临床管理
洪天配教授指出,对于 T2DM 来说,CKD 带来的是双重危害[3]:一是加速了糖尿病事件链的进展,从血压、血脂、蛋白尿等多重危险因素,到心血管并发症等靶器官损害,再到心肾事件的发生;二是加速慢性肾病进程,使得患者快速进入终末期肾病(ESKD)阶段甚至死亡(图 1)。
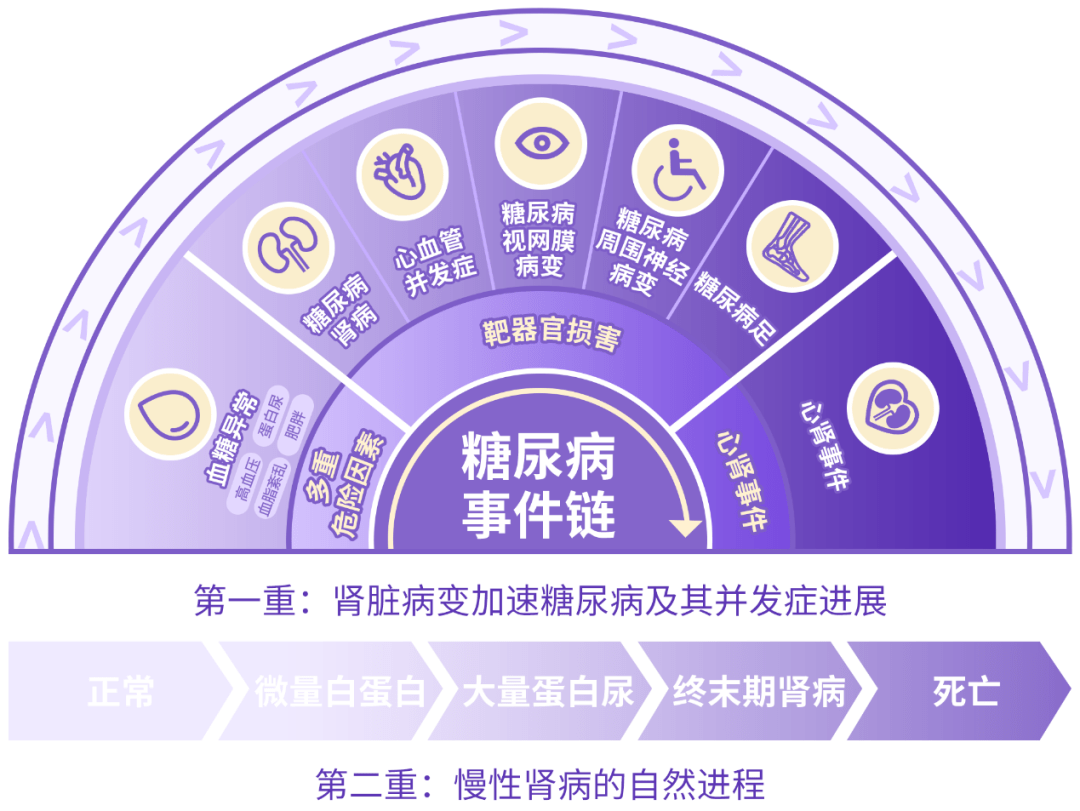
图 1 肾脏病变对于 T2DM 的双重危害[3]
研究表明,糖尿病患者一旦合并 CKD,心血管死亡和全因死亡风险成倍增加[4]。那么,此类患者如何进行有效管理?
早筛查早干预,兼顾危险因素管理
有利于肾功能改善
洪天配教授进一步指出,蛋白尿是识别早期肾脏病变的敏感性指标[5],是 CKD 快速进展的预测因子[6]。随着尿白蛋白/尿肌酐(UACR)的增加,糖尿病患者进展为 ESKD 风险显著增加[5]。在早期蛋白尿阶段肾功能仍可逆[7],如能把握这个关键时间窗,早筛查早干预,可改善患者预后。
然而,糖尿病患者 CKD 的筛查诊断率低。在美国,65 岁及以上的糖尿病患者中进行尿蛋白检测的仅占 41.8%[8],T2DM 患者中 CKD G1~3 期的诊断率分别为 1.1%、4.9% 和 18%[9],因此洪天配教授认为应根据指南建议(图 2)[10],推动早期筛查刻不容缓。
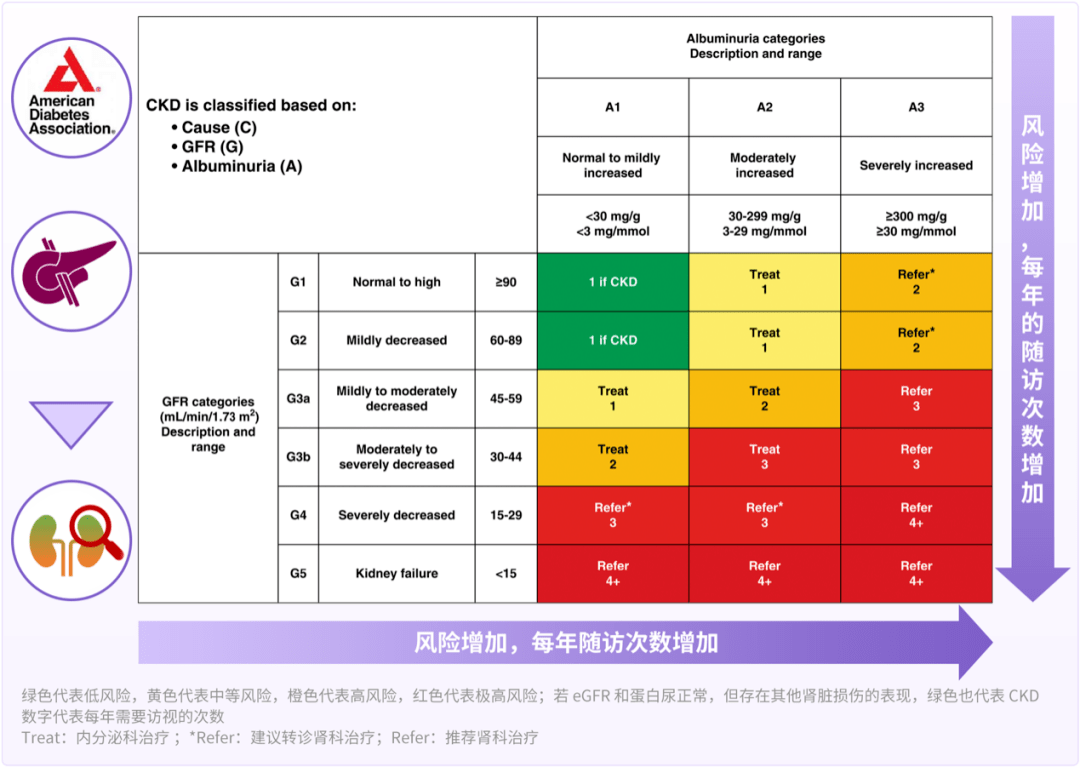
图 2 2023 版美国糖尿病学会(ADA)指南 糖尿病合并 CKD 筛查建议[10]
在 T2DM 合并 CKD 的早期干预方面,洪天配教授强调需兼顾危险因素管理与肾功能改善,即综合管理高血糖、高血压、肥胖、蛋白尿等多重危险因素,以及延缓和逆转蛋白尿,改善肾功能。
标本兼顾,多措并举
SGLT2i 助力 T2DM 合并 CKD 早期管理
近年来,钠葡萄糖协同转运蛋白 2 抑制剂(SGLT2i)多个大型临床研究结果的公布,为 T2DM 合并 CKD 的早期管理带来了新证据。洪天配教授以达格列净为例做了进一步讲解:
改善多重危险因素
SGLT2i 可改善 T2DM 患者血糖、血压、体重等多重危险因素。研究表明,达格列净 10 mg 可降低 T2DM 患者糖化血红蛋白(HbA1c)1.45%,与二甲双胍 2,000 mg 疗效相当[11];同时,在联合二甲双胍的基础上,达格列净 5 mg 可降低 T2DM 患者体重达 2.9 kg(安慰剂组降低 0.9 kg),达格列净 10 mg 降低收缩压达 5.1 mmHg(安慰剂组降低 0.2 mmHg)[12]。。
扩展阅读:
与安慰剂相比,恩格列净 10 mg 降低 T2DM 患者 HbA1c 达 0.74%,降低体重约 2 kg,降低收缩压约 4.6 mmHg[13];与安慰剂相比,卡格列净 300 mg 降低 T2DM 患者 HbA1c 1.16%,降低体重 2.9 kg,降低收缩压 5.4 mmHg 和舒张压 2.0 mmHg[14];与安慰剂相比,恒格列净 10 mg 降低 T2DM 患者 HbA1c 0.94%,体重 1.5 kg,收缩压 4.4 mmHg 和舒张压 1.7 mmHg[15]。
(上下滑动查看更多)
有效减少蛋白尿,延缓肾病进展
SGLT2i 有效减少 T2DM 合并 CKD 患者的蛋白尿,进而延缓肾病进展。
一项事后分析[16]纳入 166 例 T2DM 合并 CKD G3 期患者,分别接受达格列净 10 mg(n = 56)、达格列净 5 mg(n = 53)和安慰剂组(n = 57)治疗,研究表明,大约 4 周时,达格列净治疗组 UACR 较基线有明显下降,且效果持续到第 104 周,达格列净 10 mg 最终降低 UACR 达 43.9%(图 3)。
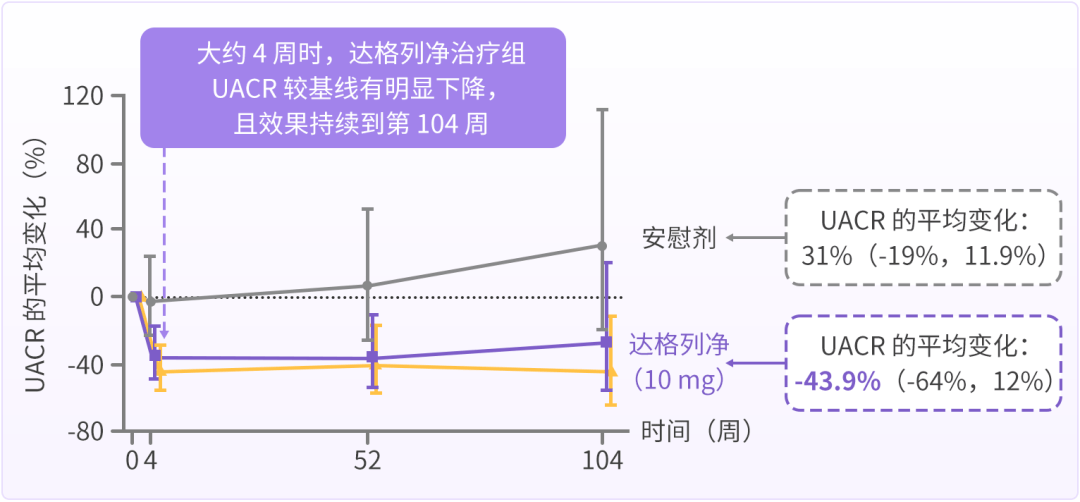
图 3 达格列净持续降低 T2DM 合并 CKD G3 期患者 UACR[16]
全球多中心、随机双盲、安慰剂对照的 DAPA-CKD 研究[17]也表明,达格列净较安慰剂显著降低合并 T2DM 的 CKD 患者的 UACR 35.1%(95% CI 30.6%~39.4%,P < 0.001)(图 4)。
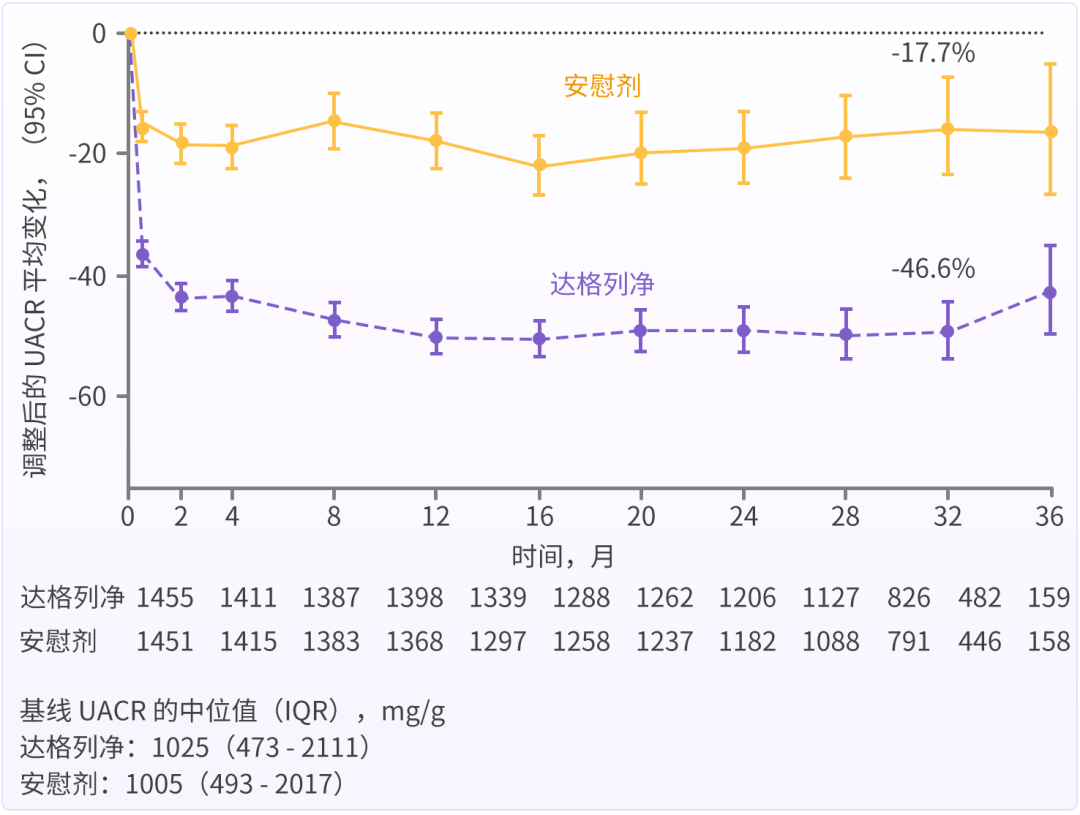
图 4 达格列净较安慰剂显著降低 T2DM 合并 CKD 患者 UACR 水平[17]
扩展阅读:
EMPA-KIDNEY 研究表明[18],恩格列净与安慰剂相比可将 T2DM 合并 CKD 患者的肾病进展(ESKD、eGFR 持续下降至 < 10 mL/min/1.73 m2、肾脏原因死亡,或随机分组后 eGFR 持续下降 ≥ 40% 或心血管死亡)的风险降低 26%(HR 0.64;95% CI 0.54~0.77);CREDENCE 研究表明[19],卡格列净较安慰剂显著降低 T2DM 合并 CKD 患者肾脏复合硬终点(ESKD、血清肌酐倍增,、肾脏或心血管死亡的复合终点)风险达 30%(HR 0.70;95% CI 0.59~0.82,P = 0.00001),显著降低肾脏特异性终点(ESKD、血清肌酐倍增,或肾脏死亡)风险达 34%(HR 0.66;95% CI 0.53~0.81,P < 0.001)。
(上下滑动查看更多)
SGLT2i 引领 CKD 治疗新变革
为 T2DM 合并 CKD 的基石用药
在 CKD 治疗的发展历程中,过去手段少且效果有限,肾素血管紧张素抑制剂(RASi)曾经带来治疗的一次革命,比如 RENAAL[20]和 IDNT 研究[21]均证实血管紧张素受体 Ⅱ 拮抗剂(ARB)可降低 T2DM 合并 CKD 患者肌酐翻倍、ESKD 或全因死亡的复合终点风险。洪天配教授介绍说,即便接受 ARB 治疗,这两项研究中糖尿病患者的肾病进展和死亡残余风险仍然分别高达 43.5% 和 35.6%[20-21]。
DAPA-CKD 研究的重磅公布,引领了 CKD 治疗二次革命。该研究结果[22]显示了达格列净能够较安慰剂显著降低肾脏硬终点[估算肾小球滤过率(eGFR)持续下降 ≥ 50%、终末期肾病,或肾脏/心血管导致的死亡]风险高达 39%(HR = 0.61,95% CI:0.51~0.72,P < 0.001),且无论是否合并糖尿病,肾脏硬终点获益一致(图 5)。
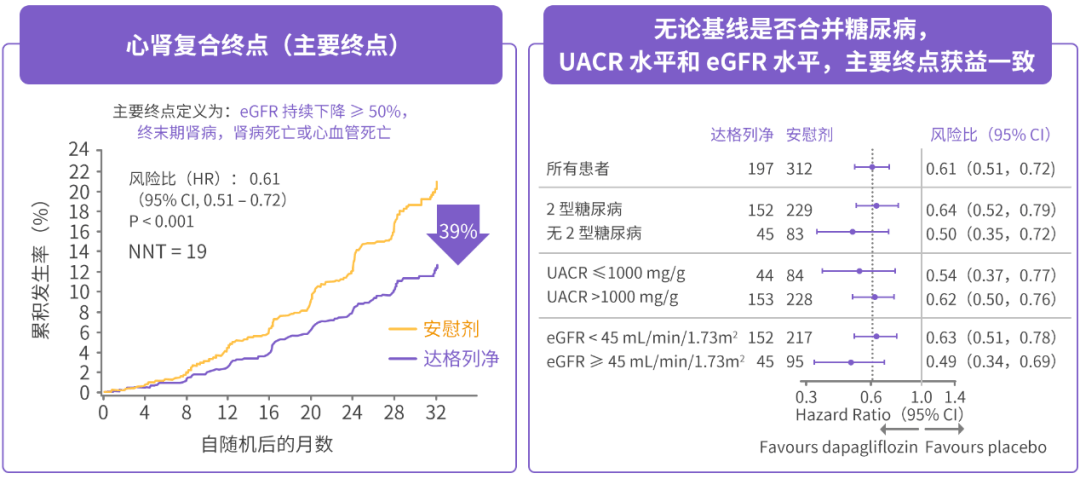
图 5 达格列净显著降低心肾复合终点风险,无论是否合并糖尿病获益一致[22]
DAPA-CKD 研究预设的亚组分析表明[17],在 T2DM 合并 CKD 人群中,达格列净显著降低心肾复合终点(eGFR 持续下降 ≥ 50%, 终末期肾病, 肾病死亡或心血管死亡)风险 36%(HR = 0.64,95% CI:0.52~0.79),显著降低肾脏特异性终点(eGFR 持续下降 ≥ 50%, 终末期肾病, 肾病死亡)风险 43%(HR = 0.57,95% CI:0.45~0.74)(图 6)。
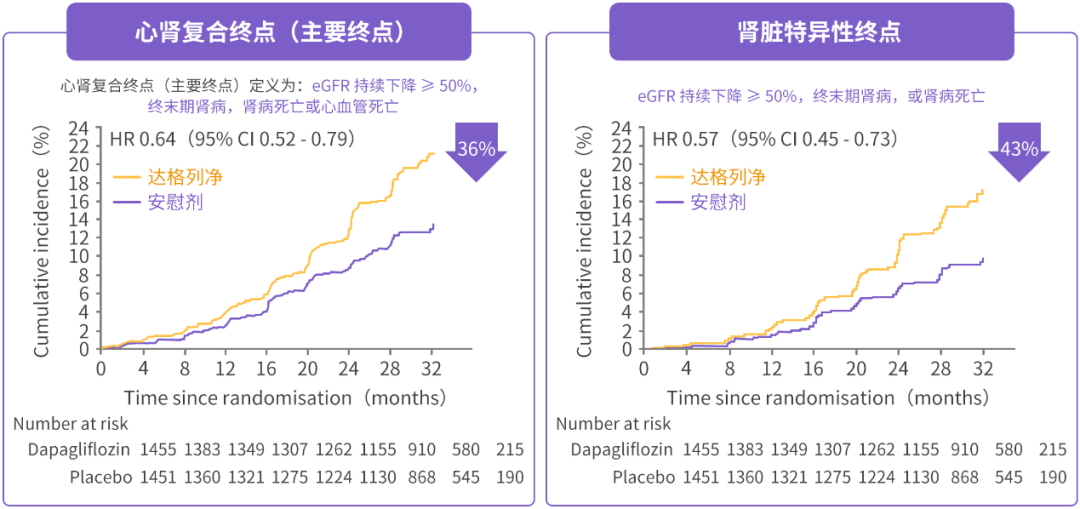
图 6 达格列净降低 T2DM 合并 CKD 患者心肾复合终点/肾脏特异性终点风险[17]
基于 DAPA-CKD 研究数据[23],安慰剂组和达格列净组进入观察终点事件的时间亦存在差异。达格列净延缓 CKD 患者进入 ESKD 时间为 6.6 年,延缓全因死亡 4.3 年[23]。
那么,SGLT2i 是如何实现肾脏获益的呢?洪天配教授从四个方面进行了解释[24-25]:
① SGLT2i 修复管球反馈,降低肾脏压力;
② SGLT2i 改善炎症和肾脏纤维化;
③ SGLT2i 降低肾脏负荷,改善缺氧;
④ SGLT2i 抑制肾素血管紧张素醛固酮系统(RAAS)活性。
基于多个循证证据,权威指南也将 SGLT2i 作为 T2DM 合并 CKD 的基石用药:
2023 版美国糖尿病学会(ADA)《糖尿病医学诊疗标准》[10]:无论 T2DM 患者是否已使用二甲双胍,无论血糖是否达标,合并动脉粥样硬化性心血管疾病(ASCVD)或 ASCVD 高风险、或心力衰竭、或 CKD 的 T2DM 患者,应以降低心肾风险为目标,给予具有明确心肾获益的 SGLT2i 治疗。
2022 年 《ADA/改善全球肾脏病预后组织(KDIGO)共识报告:慢性肾脏病患者的糖尿病管理》[26]:对于 T2DM 合并 CKD 的患者,推荐使用 SGLT2i 作为有一线治疗药物,此类药物已被证实对肾脏或心血管有益处。
总结
T2DM 合并 CKD 患病率高,患病人群庞大,带来双重危害,需早筛早治。CKD 的管理强调延缓疾病进展和降低心血管事件风险,改善血糖、血压等危险因素,同时亦需关注 CKD 并发症如肾性贫血等。以达格列净、恩格列净为代表的 SGLT2i 兼顾血糖、血压和体重管理,有效减少蛋白尿,延缓肾病进展,改善心肾结局,降低全因死亡,成为 T2DM 合并 CKD 治疗的基石。
注明:
达格列净在中国尚未获批改善糖尿病患者心血管疾病风险 / 肾脏疾病风险的适应症,尚未获批减少糖尿病患者心血管死亡或心衰住院风险的适应症;达格列净在中国尚未获得治疗肥胖 / 高血压适应症,体重降低 / 血压降低是临床研究的次要终点
声明:仅供医疗卫生专业人士参考,不得转发或分享非医疗卫生专业人士。不得用于推广目的。文中案例为虚拟案例,不作为治疗推荐。本文的采访/撰稿/发布由阿斯利康提供支持。审批编码:CN-125644 到期日:2024-12-6
调研问题

声明:仅供医疗卫生专业人士参考,不得转发或分享非医疗卫生专业人士。不得用于推广目的。本文的采访/撰稿/发布由阿斯利康提供支持
内容策划:杨琤韵
内容审核:龙瑞瑾
参考文献
[1]. Duan J, Wang C, Liu D, et al. Prevalence and risk factors of chronic kidney disease and diabetic kidney disease in Chinese rural residents: a cross-sectional survey[J]. Sci Rep, 2019, 9(1):10408.
[2]. 中华预防医学会肾脏病预防与控制专业委员会. 中国慢性肾脏病早期评价与管理指南[J]. 中华内科杂志, 2023, 62(08):902-930.
[3]. 许曼音. 糖尿病学(第二版)[M]. 上海科学技术出版社:2010.
[4]. Afkarian M, Sachs MC, Kestenbaum B, et al. Kidney disease and increased mortality risk in type 2 diabetes[J]. J Am Soc Nephrol. 2013, 24(2):302-8.
[5]. Fox CS, Matsushita K, Woodward M, Associations of kidney disease measures with mortality and end-stage renal disease in individuals with and without diabetes: a meta-analysis[J]. Lancet, 2012, 380(9854):1662-73.
[6]. Go AS, Yang J, Tan TC, et al. Contemporary rates and predictors of fast progression of chronic kidney disease in adults with and without diabetes mellitus[J]. BMC Nephrol, 2018, 19(1):146.
[7]. Dzau V. The cardiovascular continuum and renin-angiotensin-aldosterone system blockade[J]. J Hypertens Suppl, 2005, 23(1):S9-17.
[8]. United States renal data system. Annual data report, 2018, 1:29-44.
[9]. Szczech LA, Stewart RC, Su HL, et al. Primary care detection of chronic kidney disease in adults with type-2 diabetes: the ADD-CKD Study (awareness, detection and drug therapy in type 2 diabetes and chronic kidney disease)[J]. PloS One, 2014, 9(11):e110535.
[10]. ADA. Standards of Medical Care in Diabetes—2023[J]. Diabetes Care, 2023, 46(Suppl 1):S1-S291.
[11]. Henry RR, Murray AV, Marmolejo MH, et al. Dapagliflozin, metformin XR, or both: initial pharmacotherapy for type 2 diabetes, a andomized controlled trial[J]. Int J Clin Pract, 2012, 66(5):446-56.
[12]. Bailey CJ, Gross JL, Pieters A, et al. Effect of dapagliflozin in patients with type 2 diabetes who have inadequate glycaemic control with metformin: a andomized, double-blind, placebo-controlled trial[J]. Lancet, 2010, 375(9733):2223-33.
[13]. Roden M, Weng J, Eilbracht J, et al. Empagliflozin monotherapy with sitagliptin as an active comparator in patients with type 2 diabetes: a andomized, double-blind, placebo-controlled, phase 3 trial[J]. Lancet Diabetes Endocrinol, 2013, 1(3):208-19.
[14]. Stenlöf K, Cefalu WT, Kim KA, et al. Efficacy and safety of canagliflozin monotherapy in subjects with type 2 diabetes mellitus inadequately controlled with diet and exercise[J]. Diabetes Obes Metab, 2013, 15(4):372-82.
[15]. Lu J, Fu L, Li Y, et al. Henagliflozin monotherapy in patients with type 2 diabetes inadequately controlled on diet and exercise: a randomized, double‑blind,placebo‑controlled, phase 3 trial[J]. Diabetes Obes Metab, 2021, 23(5):1111‑1120.
[16]. Fioretto P, Stefansson BV, Johnsson E, et al. Dapagliflozin reduces albuminuria over 2 years in patients with type 2 diabetes mellitus and renal impairment[J]. Diabetologia, 2016, 59(9):2036-9.
[17]. Wheeler DC, Stefánsson BV, Jongs N, et al. Effects of dapagliflozin on major adverse kidney and cardiovascular events in patients with diabetic and non-diabetic chronic kidney disease: a prespecified analysis from the DAPA-CKD trial[J]. Lancet Diabetes Endocrinol. 2021, 9(1):22-31.
[18]. The EMPA-KIDNEY Collaborative Group, et al. Empagliflozin in Patients with Chronic Kidney Disease[J]. N Engl J Med, 2023, 388(2):117-127.
[19]. Perkovic V, Jardine MJ, Neal B, et al. Canagliflozin and Renal Outcomes in Type 2 Diabetes and Nephropathy[J]. N Engl J Med, 2019, 13;380(24):2295-2306.
[20]. Brenner BM, Cooper ME, de Zeeuw D, et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy[J]. N Engl J Med, 2001, 345(12):861-9.
[21]. Lewis EJ, Hunsicker LG, Clarke WR, et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes[J]. N Engl J Med, 2001, 345(12):851-60.
[22]. Heerspink HJL, Stefánsson BV, Correa-Rotter R, et al. Dapagliflozin in Patients with Chronic Kidney Disease[J]. N Engl J Med, 2020, 383(15):1436-1446.
[23]. Phil McEwan, et al. ESTIMATING THE IMPACT OF DELAYED DISEASE PROGRESSION AND CARDIOVASCULAR EVENT INCIDENCE ASSOCIATED WITH DAPAGLIFLOZIN BASED ON THE RESULTS OF DAPA. Presented at AMCP 2021, Virtual meeting, 12 April 2021-16 April 2021.
[24]. Heerspink HJL, Kosiborod M, Inzucchi SE, et al. Renoprotective effects of sodium-glucose cotransporter-2 inhibitors[J]. Kidney Int, 2018, 94(1):26-39.
[25]. Sano M. A new class of drugs for heart failure: SGLT2 inhibitors reduce sympathetic overactivity[J]. J Cardiol, 2018, 71(5):471-476.
[26]. ADA/KDIGO. Diabetes management in chronic kidney disease: a consensus report by the American Diabetes Association (ADA) and Kidney Disease: Improving Global Outcomes (KDIGO)[J]. Diabetes Care, 2022, 45(12):3075-3090.
